Inhaltsverzeichnis
Die Ionenbindung zählt zu den primären Bindungen. Bei dieser Bindungsart sind immer ein metallische und ein nichtmetallisches Atom beteiligt.
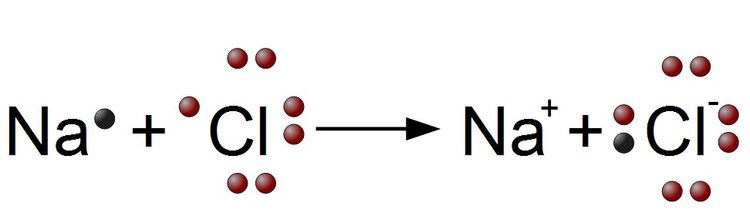
Diese beiden Atome versuchen in einen Edelgaszustand zu gelangen, indem das eine Atom ein oder mehrere Valenzelektronen an das andere Atom abgibt. Ein hierfür bekanntes Beispiel ist das Natriumchlorid, eher bekannt als Kochsalz. Natriumchlorid besteht, wie der Name schon sagt, aus Natrium und Chlor.
Beispielreaktion
Beispiel
Es besteht also eine Anziehung aufgrund der entgegengesetzten Ladung der Ionen.
Beispielreaktion
Beispiel
Merke
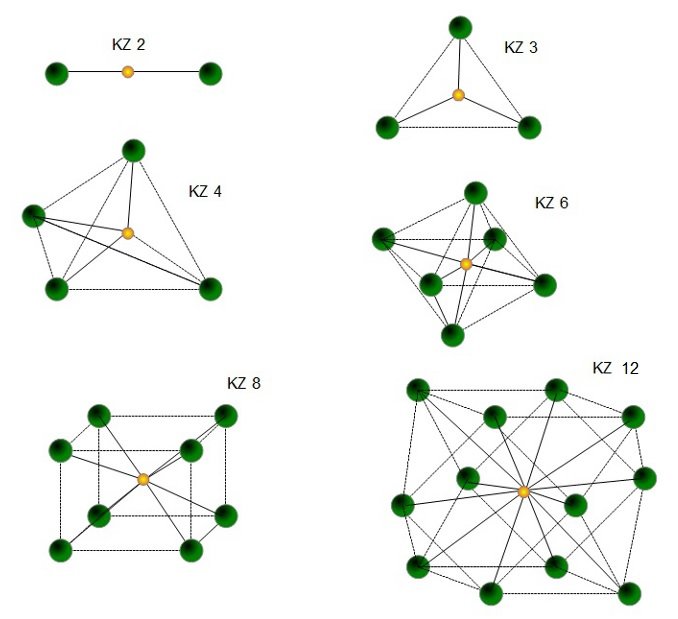
Koordinationszahl
Die Koordinationszahl beschreibt, wie viele Atome mit einem Atom im gleichen Abstand unmittelbar benachbart sind. Die Bestimmung dieser Zahl erfolgt aus dem Radienverhältnis
$\frac{r}{R} $.
Diese Berechnung ist zulässig, da sich die Radien aufgrund der Abstoßungskräfte nicht überlappen dürfen. In der folgenden Tabelle ist der Geltungsbereich der Radienverhältnisse mit den zugehörigen Koordinationszahlen aufgeführt:
| Geltungsbereich der Radienverhältnisse $\frac{r}{R}$ | Koordinationszahl KZ |
| $ 0 | 2 [Ebene Bindung] |
| $ 0,155 | 3 [Ebenes Dreieck] |
| $ 0,225 | 4 [Tetraeder] |
| $ 0,414 | 6 [Oktaeder] |
| $ 0,732 | 8 [Würfel] |
| $ \frac{r}{R} = 1 $ | 12 [Kub-Oktaeder] |
Merke
Weitere interessante Inhalte zum Thema
-
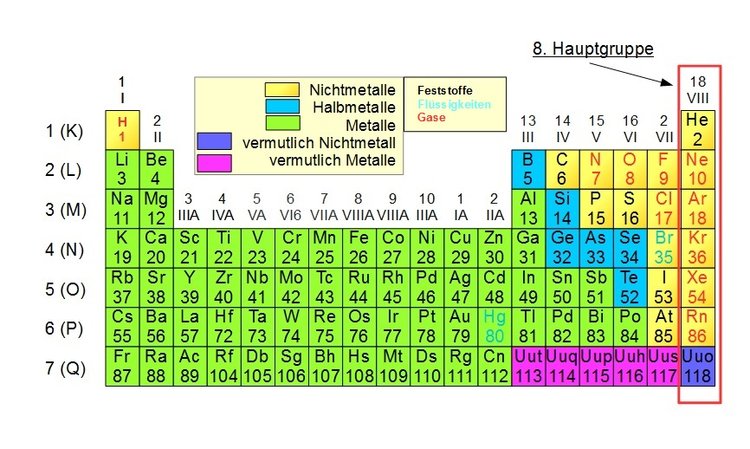
8. Hauptgruppe des PSE, Edelgase
Vielleicht ist für Sie auch das Thema 8. Hauptgruppe des PSE, Edelgase (Elemente des Periodensystems) aus unserem Online-Kurs Anorganische Chemie für Ingenieure interessant.
-
Ionenbindung, heteropolare Bindung
Vielleicht ist für Sie auch das Thema Ionenbindung, heteropolare Bindung (Bindungsarten, Bindungsstärke und Bindungslänge) aus unserem Online-Kurs Anorganische Chemie für Ingenieure interessant.